检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
检测到您当前使用浏览器版本过于老旧,会导致无法正常浏览网站;请您使用电脑里的其他浏览器如:360、QQ、搜狗浏览器的极速模式浏览,或者使用谷歌、火狐等浏览器。
 下载Firefox
下载Firefox
2026年4月30日,北京大学生命科学学院陈建国、郑鹏里、滕俊琳与北京大学未来技术学院刘贝课题组合作在Nature Communications上发表了题为“Acetylation of STX17 promotes its autophagosomal translocation”的研究论文。该研究首次严谨证实自噬关键SNARE蛋白STX17源自胞质库、并经乙酰化-去乙酰化动态修饰与肌动蛋白马达协同完成自噬体靶向转运,为理解自噬晚期调控提供了关键机制。
自噬(autophagy)是真核细胞维持内环境稳态的重要过程,其通过形成双层膜结构的自噬体(autophagosome)包裹细胞内损伤的细胞器或蛋白聚集体,与溶酶体融合完成降解。在这一过程中,自噬体与溶酶体的融合是决定自噬功能是否完成的关键步骤。SNARE蛋白STX17是介导该融合过程的核心因子,其在静息状态下广泛分布于内质网、线粒体及胞质等多个部位;而当自噬激活时,大量STX17会转移到自噬体膜上。但其究竟从何而来、如何被招募到自噬体、又受哪些因子精确调控,一直是领域内尚未完全阐明的重要问题。
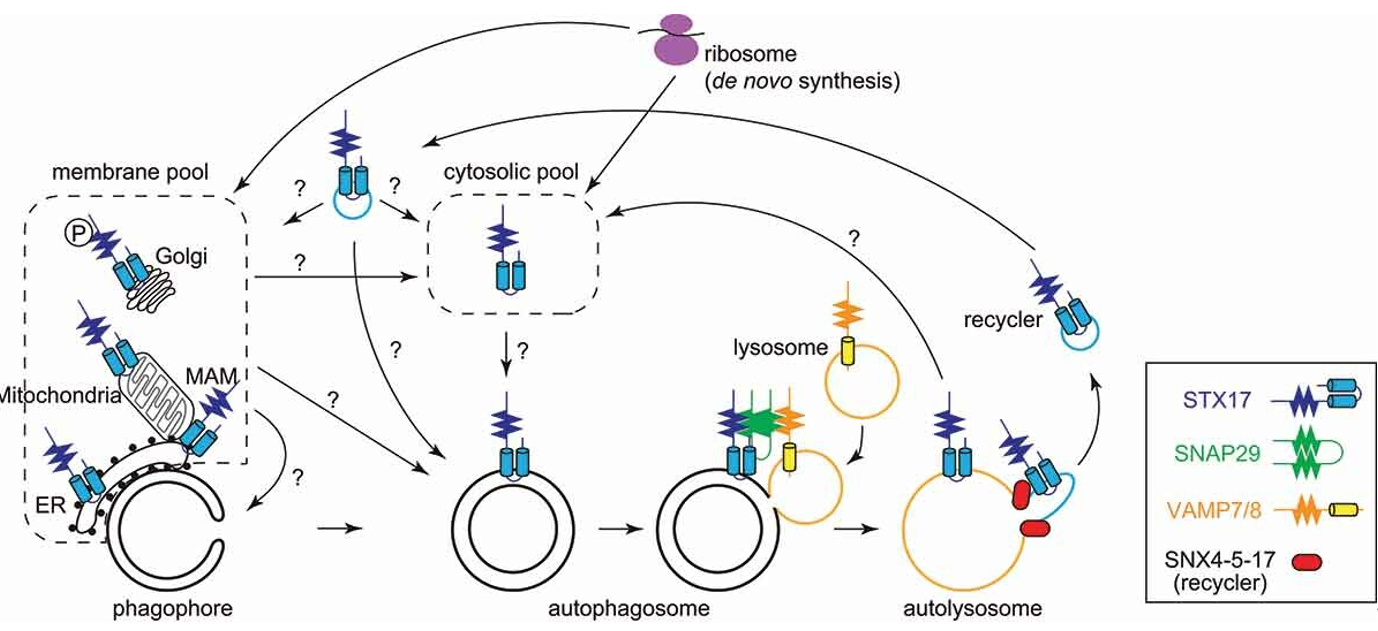
图1:STX17转运模型1
本研究利用CRISPR敲入细胞、亚细胞组分分离、体外重构和单分子追踪等方法,首次明确证实:向自噬体转运的功能性STX17主要来自胞质库,而非细胞器膜库,为理解其转运机制奠定了关键的定位基础。
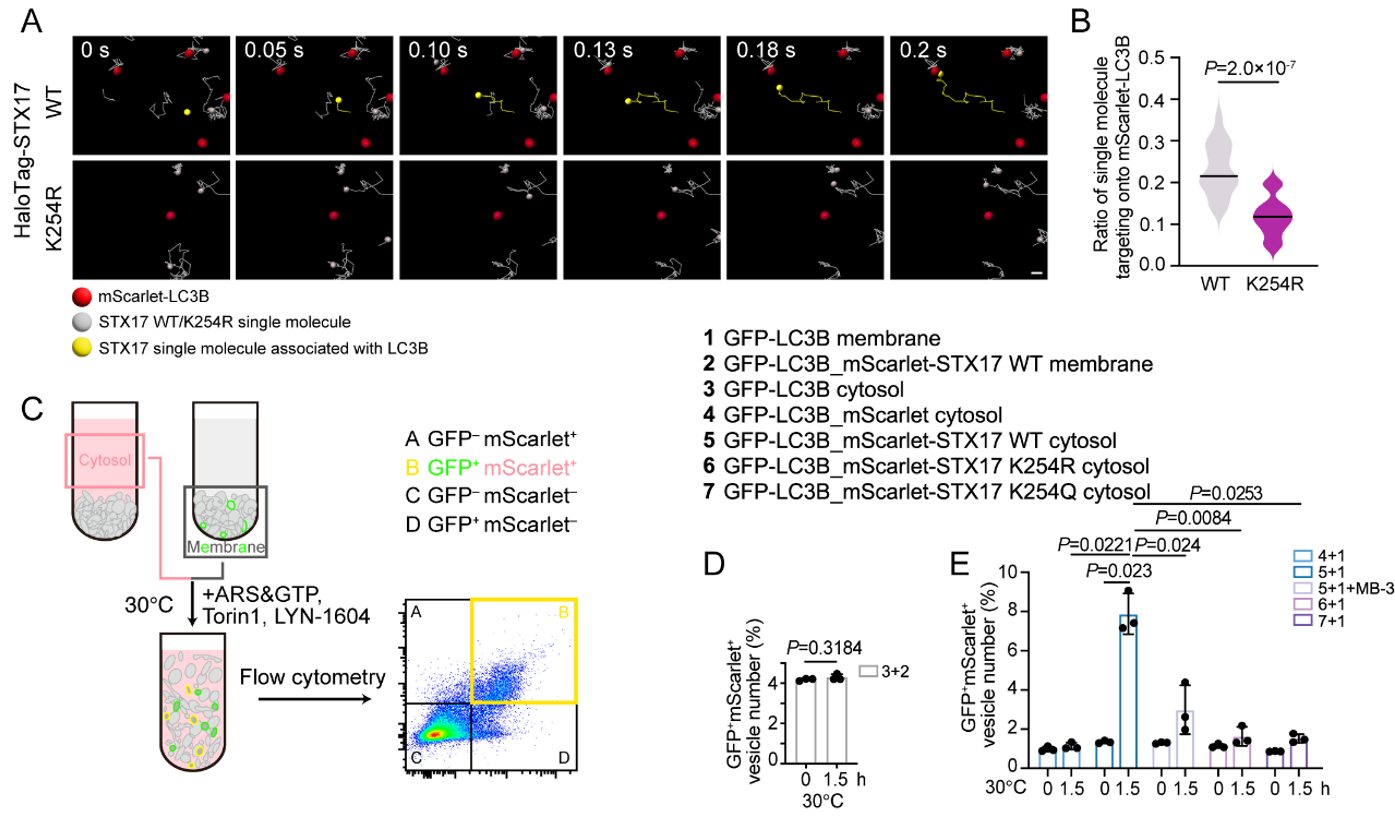
图2:STX17 K254乙酰化修饰促进其从胞质库转运到自噬体
图A-B:单分子追踪检测发现抑制K254位点乙酰化修饰下调STX17转运到自噬体;图C-E:STX17在体外重构实验中从胞质库转运到自噬体膜。
为揭示其背后的分子机制,研究团队通过蛋白质修饰质谱等手段,发现饥饿诱导自噬时,STX17第254位赖氨酸(K254)会发生特异性乙酰化修饰。该修饰由乙酰转移酶GCN5催化,并可被去乙酰化酶SIRT1逆转,形成动态可逆的精准调控。进一步实验表明,K254乙酰化显著增强STX17与肌动蛋白依赖的马达蛋白MYO6的相互作用,进而促进胞质STX17向自噬体的转运过程。
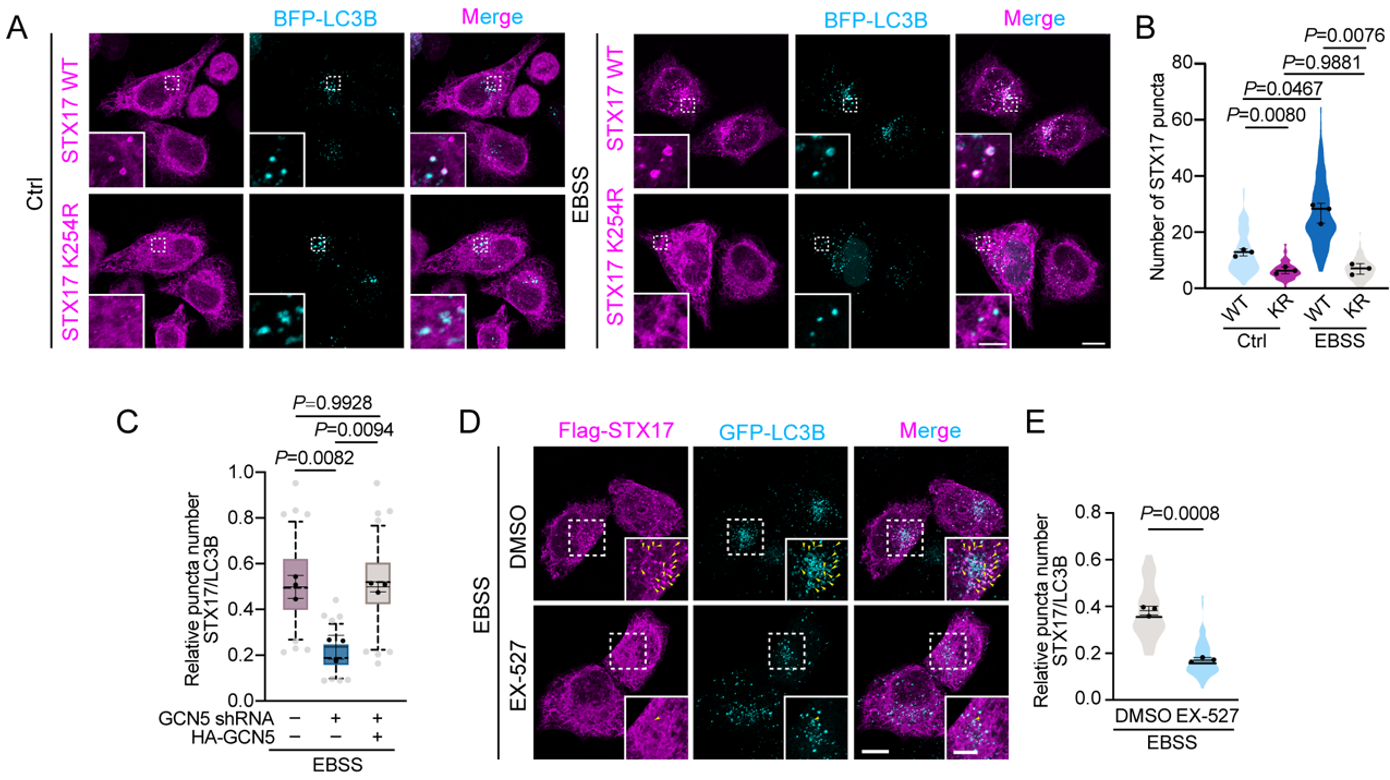
图3:A-B:STX17 K254乙酰化对其在饥饿条件下定位到自噬体至关重要;C-D:GCN5和SIRT1调控STX17在自噬体的定位。
该工作阐明了乙酰化-去乙酰化修饰如何作为关键开关,调控STX17从胞质到自噬体的转运,并揭示了马达蛋白MYO6在这一过程中的重要作用,完善了自噬体-溶酶体融合的上游调控通路。
自噬功能异常与神经退行性疾病、肿瘤、代谢疾病等多种人类疾病密切相关。本研究揭示的GCN5–SIRT1–STX17–MYO6调控轴,为深入理解自噬晚期步骤的精密调控提供了新的分子基础,也为相关疾病的机制研究与潜在干预靶点探索提供了理论支撑。
北京大学生命科学学院陈建国教授、郑鹏里研究员、滕俊琳教授和未来技术学院刘贝研究员为本文的共同通讯作者。北京大学生科院周晨倩博士为论文第一作者,未来技术学院李沛洋,北京大学生科院程怡茹、胡迎春和王婧子在本研究中做出了重要贡献。该研究得到了国家自然科学基金等项目的支持。
原文链接:https://www.nature.com/articles/s41467-026-72476-8
参考文献:
1. Koyama-Honda, I. & Mizushima, N. Transient visit of STX17 (syntaxin 17) to autophagosomes. Autophagy 18, 1213–1215 (2022).